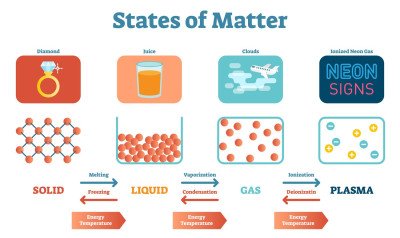
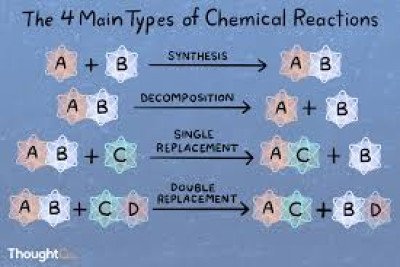
Chemical Bonding and Molecular Structure
Chemical bonding is one of the most basic fundamentals of chemistry that explains other concepts such as molecules and reactions. সায়নিক বন্ধন হল রসায়নের অন্যতম মৌলিক মৌলিক বিষয় যা অন্যান্য ধারণা যেমন অণু এবং প্রতিক্রিয়া ব্যাখ্যা করে।
English
Last updated
Mon, 23-Mar-2026